397 голосов «за» и 0 «против» — таковы результаты голосования в Госдуме за проект закона, предусматривающего появление новой процедуры для производителей ветеринарных препаратов. 16 июня депутаты приняли в третьем чтении закон «О внесении изменений в Федеральный закон «Об обращении лекарственных средств».
Идея введения новой процедуры появилась в стенах Госдумы в марте 2020-го, но проект был отклонен. В ноябре был внесен новый аналогичный проект, судьба которого оказалась более успешной, несмотря на то что он вводит дополнительную процедуру в сферу, и без того изобилующую контрольными действиями. Принятый проект дополняет ФЗ-61 новой статьей «Ввод в гражданский оборот лекарственных препаратов для ветеринарного применения».
В ней говорится, что перед вводом в гражданский оборот каждой серии (за исключением иммунобиологических) российский производитель (или организация, осуществляющая ввоз иностранных лекарств) представляет в Россельхознадзор документ, подтверждающий соответствие качества требованиям, установленным при его государственной регистрации, а также подтверждение уполномоченного лица производителя соответствия препарата требованиям, установленным при регистрации. При этом иностранные производители также должны иметь заключение о соответствии требованиям правил надлежащей производственной практики.
Уполномоченное держателем или владельцем регистрационного удостоверения лицо, о котором идет речь, должно быть аттестовано и иметь стаж работы не менее 5 лет в области производства и (или) контроля качества лексредств либо в области мониторинга эффективности и безопасности ветпрепаратов, проводимого держателем или владельцем регистрационного удостоверения либо уполномоченным ими юрлицом, а также высшее образование по одной из специальностей: биология, биотехнология, ветеринария, ветеринарно-санитарная экспертиза, клиническая медицина, радиационная, химическая и биологическая защита, фармация, фундаментальная медицина, химическая технология, химия.
Для первых двух серий ветеринарного препарата, впервые произведенного в России или впервые ввозимого в нашу страну, Россельхознадзор также требует протоколы испытаний о соответствии этих серий показателям качества, предусмотренным нормативным документом (протокол испытаний), проводимых аккредитованными в соответствии с законодательством РФ испытательными лабораториями (центрами).
Ежегодно не позднее 1 февраля производители или импортеры представляют в Россельхознадзор протокол испытаний поступившего в течение года в гражданский оборот препарата (на одну серию каждого торгового наименования с учетом лекарственной формы, а для не являющегося иммунобиологическим препарата также с учетом дозировки), проводимых аккредитованными лабораториями.
Ввод в гражданский оборот иммунобиологического препарата осуществляется на основании разрешения Россельхознадзора, которое выдается на основании протокола испытаний, проводимых аккредитованными организациями, подведомственными Минсельхозу или Россельхознадзору, а также перечисленных ранее документов. Срок выдачи такого разрешения — пять рабочих дней со дня представления документов производителем или импортером. Такое разрешение выдается в отношении каждой из первых двух серий иммунобиологического препарата, впервые произведенного или ввозимого в Россию. Такое разрешение выдается на весь срок обращения серии. В отношении последующих серий такое разрешение выдается сроком на три года.
Представление перечисленных документов и сведений не требуется в отношении препаратов, предназначенных для вывоза из РФ, проведения доклинических или клинических исследований, а также образцов, предназначенных для проведения экспертизы для государственной регистрации или внесения изменений в регистрационное досье.
Федеральный закон вступит в силу с 1 сентября 2023 года. Действие новых положений № 61-ФЗ «Об обращении лекарственных средств» не распространяется на серии лекарственных препаратов для ветеринарного применения, введенные в гражданский оборот на территории Российской Федерации до дня вступления в силу настоящего Федерального закона.
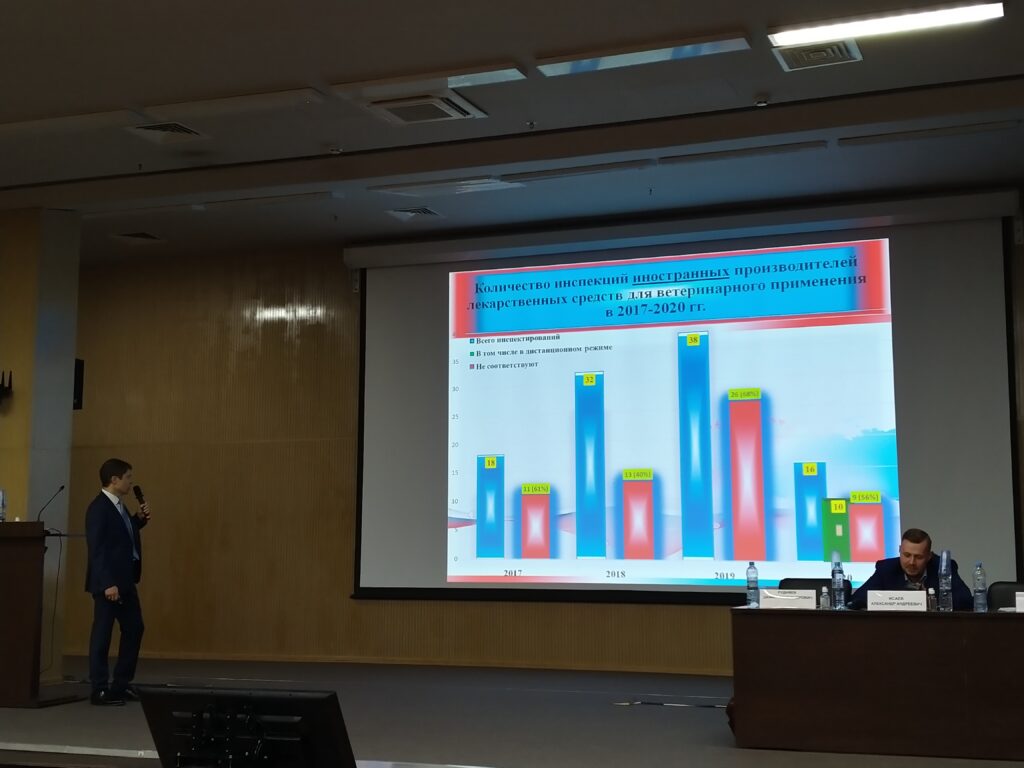
Особую тревогу в новом законе вызывает обязательное наличие GMP-сертификата у иностранных производителей — сейчас, когда пандемия наложила вынужденные ограничения на поездки. Вопрос проведения GMP-инспекций поднимался на конференции «Актуальные вопросы обращения лекарственных средств для ветеринарного применения, профилактики и лечения инфекционных болезней продуктивных животных», которая прошла 17 июня в рамках деловой программы выставки «MVC: Зерно–Комбикорма–Ветеринария 2021». Данил Рудняев, заместитель директора, руководитель органа инспекции ФГБУ «ВГНКИ», подвел итоги четырех лет инспектирования иностранных производителей.
Он привел статистику по проведенным инспекциям и рассмотрел меняющееся законодательство в этой сфере. В частности, в постановлении Правительства РФ от 03.12.2015 № 1314 «Об определении соответствия производителей лекарственных средств требованиям правил надлежащей производственной практики» введена норма о возможности предоставления плана корректирующих и предупреждающих действий (CAPA).
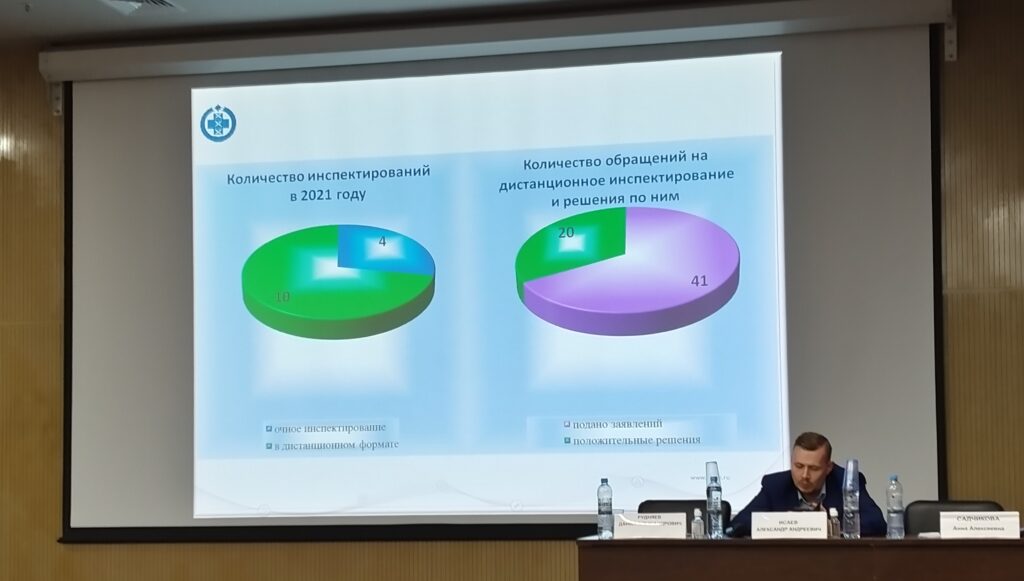
Еще одним нововведением стала возможность проведения инспектирования в дистанционном формате. Однако Рудняев отметил, что такой формат возможен не для всех производителей: например, дистанционно невозможно оценить производство иммунобиологической продукции. Между тем в 2020-м были проведены дистанционно 10 инспекций иностранных производителей и 18 — отечественных. Некоторым иностранным производителям удается вывести российских инспекторов на предприятия. В частности, были проведены два выезда в Бразилию, инспекции площадок в Венгрии и Италии.